Neurodegeneratiiviset sairaudetAivojen tai selkäytimen tiettyjen haavoittuvien hermosolupopulaatioiden etenevä tai pysyvä menetys. NDD-sairauksien luokittelu voi perustua useisiin kriteereihin, mukaan lukien neurodegeneraation anatominen jakauma (kuten ekstrapyramidaaliset häiriöt, frontotemporaalinen rappeuma tai spinocerebellaariset ataksiat), primaariset molekyylipoikkeavuudet (kuten amyloid-β, prionit, tau tai α-synukleiini) tai tärkeimmät kliiniset piirteet (kuten Parkinsonin tauti, amyotrofinen lateraaliskleroosi ja dementia). Näistä luokittelu- ja oireesityseroista huolimatta sairauksilla, kuten Parkinsonin taudilla (PD), amyotrofisella lateraaliskleroosilla (ALS) ja Alzheimerin taudilla (AD), on yhteisiä taustalla olevia prosesseja, jotka johtavat hermosolujen toimintahäiriöihin ja lopulta solukuolemaan.
Maailman terveysjärjestö WHO arvioi, että vuoteen 2040 mennessä näistä sairauksista tulee toiseksi yleisin kuolinsyy kehittyneissä maissa, sillä miljoonia ihmisiä maailmanlaajuisesti kärsii neurodegeneratiivisista sairauksista. Vaikka tiettyihin sairauksiin liittyvien oireiden lievittämiseen ja hallintaan on olemassa useita hoitoja, tehokkaita menetelmiä näiden sairauksien etenemisen hidastamiseksi tai parantamiseksi on edelleen vaikea löytää. Viimeaikaiset tutkimukset osoittavat hoitoparadigmojen muuttuvan pelkästä oireenmukaisesta hoidosta solujen suojamekanismien hyödyntämiseen tilan pahenemisen estämiseksi. Laajat todisteet viittaavat siihen, että oksidatiivisella stressillä ja tulehduksella on keskeinen rooli neurodegeneraatiossa, mikä asettaa nämä mekanismit kriittisiksi kohteiksi solujen suojaukselle. Viime vuosina perustutkimus ja kliininen tutkimus ovat paljastaneet hyperbaarisen happihoidon (HBOT) potentiaalin neurodegeneratiivisten sairauksien hoidossa.
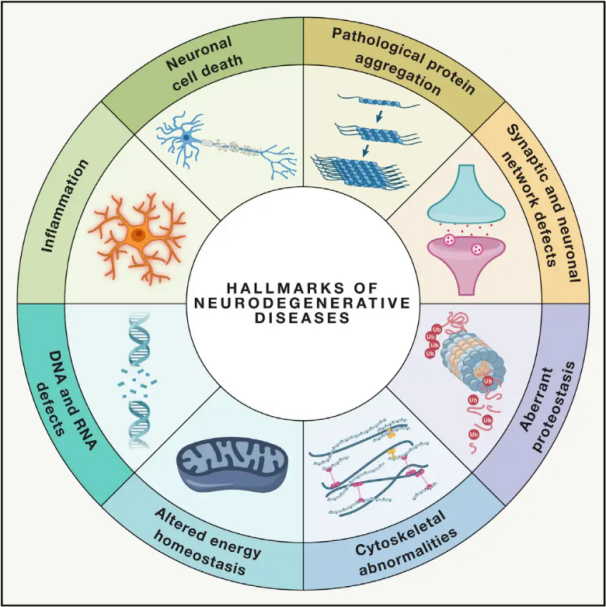
Hyperbaarisen happihoidon (HBOT) ymmärtäminen
HBOT-hoidossa painetta nostetaan tyypillisesti yli yhden absoluuttisen ilmakehän (ATA) paineeseen – merenpinnan paineeseen – 90–120 minuutin ajaksi, ja se vaatii usein useita hoitokertoja hoidettavasta tilasta riippuen. Lisääntynyt ilmanpaine parantaa hapen kulkeutumista soluihin, mikä puolestaan stimuloi kantasolujen lisääntymistä ja tehostaa tiettyjen kasvutekijöiden välittämiä paranemisprosesseja.
Alun perin HBOT:n soveltaminen perustui Boyle-Marriottin lakiin, joka olettaa paineesta riippuvan kaasukuplien vähenemisen sekä kudosten korkeiden happitasojen hyötyjä. On olemassa useita patologioita, joiden tiedetään hyötyvän HBOT:n tuottamasta hyperoksisesta tilasta, mukaan lukien nekroottiset kudokset, säteilyvammat, traumat, palovammat, osasto-oireyhtymä ja kaasukuolio, muiden Undersea and Hyperbaric Medical Societyn listaamien sairauksien joukossa. HBOT on osoitettu tehokkaaksi myös lisähoitona useissa tulehdus- tai tartuntatautimalleissa, kuten koliitissa ja sepsiksessä. Tulehdusta estävien ja oksidatiivisten mekanismiensa ansiosta HBOT tarjoaa merkittävää potentiaalia neurodegeneratiivisten sairauksien hoitomuotona.
Hyperbaarisen happihoidon prekliiniset tutkimukset neurodegeneratiivisissa sairauksissa: Näkemyksiä 3×Tg-hiirimallista
Yksi merkittävimmistä tutkimuksistakeskittyi Alzheimerin taudin (AD) 3×Tg-hiirimalliin, joka osoitti HBOT:n terapeuttisen potentiaalin kognitiivisten häiriöiden lievittämisessä. Tutkimukseen osallistui 17 kuukauden ikäisiä 3×Tg-uroshiiriä verrattuna 14 kuukauden ikäisiin C57BL/6-uroshiiriin, jotka toimivat kontrollina. Tutkimus osoitti, että HBOT ei ainoastaan parantanut kognitiivista toimintaa, vaan myös vähensi merkittävästi tulehdusta, plakkikuormitusta ja Tau-fosforylaatiota – Alzheimerin taudin patologiaan liittyvää kriittistä prosessia.
HBOT:n suojaavien vaikutusten katsottiin johtuvan neuroinflammaation vähenemisestä. Tämä ilmeni mikrogliasolujen proliferaation, astroglioosin ja tulehdusta edistävien sytokiinien erityksen vähenemisenä. Nämä havainnot korostavat HBOT:n kaksoisroolia kognitiivisen suorituskyvyn parantamisessa ja samanaikaisesti Alzheimerin tautiin liittyvien neuroinflammatoristen prosessien lieventämisessä.
Toisessa prekliinisessä mallissa käytettiin 1-metyyli-4-fenyyli-1,2,3,6-tetrahydropyridiini (MPTP) -hiiriä HBOT:n hermosolujen toimintaan ja motorisiin kykyihin kohdistuvien suojamekanismien arvioimiseksi. Tulokset osoittivat, että HBOT edisti näiden hiirten motorisen aktiivisuuden ja otteen voimakkuuden paranemista, mikä korreloi mitokondrioiden biogeneesisignaloinnin lisääntymisen kanssa, erityisesti SIRT-1:n, PGC-1α:n ja TFAM:n aktivaation kautta. Tämä korostaa mitokondrioiden toiminnan merkittävää roolia HBOT:n hermosoluja suojaavissa vaikutuksissa.
HBOT:n mekanismit neurodegeneratiivisissa sairauksissa
HBOT:n käytön perusperiaate neurodegeneratiivisissa sairauksissa on vähentyneen hapensaannin ja neurodegeneratiivisten muutosten alttiuden välinen suhde. Hypoksian indusoima tekijä 1 (HIF-1) on keskeinen transkriptiotekijä, joka mahdollistaa solujen sopeutumisen alhaiseen happipaineeseen. Sen on osoitettu liittyvän useisiin neurodegeneratiivisiin sairauksiin, kuten Alzheimerin tautiin, Parkinsonin tautiin, Huntingtonin tautiin ja ALS:ään, mikä tekee siitä tärkeän lääkekohteen.
Koska ikä on merkittävä riskitekijä useille neurodegeneratiivisille sairauksille, HBOT:n vaikutuksen tutkiminen ikääntymisen neurobiologiaan on elintärkeää. Tutkimukset ovat osoittaneet, että HBOT voi parantaa ikään liittyviä kognitiivisia häiriöitä terveillä iäkkäillä koehenkilöillä.Lisäksi iäkkäillä potilailla, joilla oli merkittäviä muistihäiriöitä, havaittiin kognitiivisia parannuksia ja lisääntynyttä aivoverenkiertoa HBOT-altistuksen jälkeen.
1. HBOT:n vaikutus tulehdukseen ja oksidatiiviseen stressiin
HBOT on osoittanut kyvyn lievittää neuroinflammaatiota potilailla, joilla on vaikea aivojen toimintahäiriö. Sillä on kyky vähentää tulehdusta edistävien sytokiinien (kuten IL-1β, IL-12, TNFα ja IFNγ) määrää samalla kun se lisää tulehdusta estävien sytokiinien (kuten IL-10) määrää. Jotkut tutkijat ehdottavat, että HBOT:n tuottamat reaktiiviset happilajit (ROS) välittävät useita hoidon hyödyllisiä vaikutuksia. Näin ollen HBOT:n paineesta riippuvan kuplia vähentävän vaikutuksen ja korkean kudoshappisaturaation saavuttamisen lisäksi siihen liittyvät positiiviset tulokset riippuvat osittain tuotettujen ROS:ien fysiologisista rooleista.
2. HBOT:n vaikutukset apoptoosiin ja neuroprotektioon
Tutkimukset ovat osoittaneet, että HBOT voi vähentää p38-mitogeeniaktivoituneen proteiinikinaasin (MAPK) fosforylaatiota hippokampuksessa, mikä parantaa kognitiivisia toimintoja ja vähentää hippokampuksen vaurioita. Sekä yksinään että yhdessä ginkgo biloba -uutteen kanssa käytettynä on havaittu vähentävän Bax-geenin ilmentymistä ja kaspaasi-9/3:n aktiivisuutta, mikä johtaa aβ25-35:n indusoiman apoptoosin vähenemiseen jyrsijämalleissa. Lisäksi toisessa tutkimuksessa osoitettiin, että HBOT-esikäsittely indusoi toleranssia aivoiskemiaa vastaan, ja mekanismeihin kuului lisääntynyt SIRT1-ilmentymä sekä lisääntyneet B-solulymfooma 2:n (Bcl-2) tasot ja vähentynyt aktiivinen kaspaasi-3, mikä korostaa HBOT:n neuroprotektiivisia ja antiapoptoottisia ominaisuuksia.
3. HBOT:n vaikutus verenkiertoon jaNeurogeneesi
HBOT-hoitoon on liitetty useita vaikutuksia kallon verisuonijärjestelmään, mukaan lukien veri-aivoesteen läpäisevyyden parantaminen, angiogeneesin edistäminen ja turvotuksen vähentäminen. Kudosten hapensaannin lisäämisen lisäksi HBOTedistää verisuonten muodostumistaaktivoimalla transkriptiotekijöitä, kuten verisuonten endoteelikasvutekijää, ja stimuloimalla hermostollisten kantasolujen lisääntymistä.
4. HBOT:n epigeneettiset vaikutukset
Tutkimukset ovat osoittaneet, että ihmisen mikrovaskulaaristen endoteelisolujen (HMEC-1) altistuminen hyperbaariselle hapelle säätelee merkittävästi 8 101 geeniä, mukaan lukien sekä ylös- että alaspäin säädeltyä ilmentymistä, mikä korostaa antioksidanttivasteen reitteihin liittyvän geenien ilmentymisen lisääntymistä.
Johtopäätös
HBOT-hoidon käyttö on ajan myötä kehittynyt merkittävästi, mikä on osoittanut sen saatavuuden, luotettavuuden ja turvallisuuden kliinisessä käytännössä. Vaikka HBOT-hoitoa on tutkittu NDD-sairauksien hoitoon muualla kuin myyntiluvassa ja siitä on tehty jonkin verran tutkimusta, on edelleen kiireellistä tehdä perusteellisia tutkimuksia HBOT-käytäntöjen standardoimiseksi näiden sairauksien hoidossa. Lisätutkimukset ovat välttämättömiä optimaalisten hoitotiheyksien määrittämiseksi ja potilaille hyödyllisten vaikutusten laajuuden arvioimiseksi.
Yhteenvetona voidaan todeta, että ylipainehappihoidon ja neurodegeneratiivisten sairauksien yhtymäkohta osoittaa lupaavia terapeuttisten mahdollisuuksien avauksia, jotka edellyttävät jatkuvaa tutkimusta ja validointia kliinisissä olosuhteissa.
Julkaisun aika: 16.5.2025

